郑州源创基因科技有限公司成立于2016年,由哥伦比亚大学博士后赵辉,归国创办的国家高新技术企业。拥有97项知识产权及实用技术,业务遍布上海、重庆、深圳、北京等城市,总部在郑州航空港区。
生活中经常听到器官移植、细胞回输需要配型,等待配型结果等词语。全世界有70多亿人口,配型成功异常困难,以骨髓造血干细胞移植为例,配型成功率在几万至几十万分之一不等。如今,医学界提出胎盘、脐带间充质干细胞使用无需配型的说法,这所谓的“配型”,究竟指的是什么?
01、什么是配型?
配型,又称组织配型,核心为HLA分型匹配。HLA 是Human Leukocyte Antigen的简拼,即“人类白细胞抗原”,广泛分布于机体内几乎所有有核细胞的表面

每个人的HLA千差万别,因此,HLA又有人体生物学的“身份证”之称。它是不同个体免疫细胞相互识别的标志,机体“区分敌我、识别自身、排除异己”的主要遗传标记,参与免疫应答反应,具有非常重要的生物学功能。
因此在接受细胞技术时,供受者之间的HLA匹配程度反映了供受双方的组织相容性程度,和移植手术后的排斥反应率密切相关,决定了移植成功或失败,故又将其称为移植抗原。
而编码这三个抗原的基因位于两条同源染色体上,一条来自父方,一条来自母方,因此,共3×2=6个位点。这也就产生了我们常听到的“全相合、4个位点相合、5个位点相合”这样的说法。
国内外大量的临床研究结果表明,受者和供者之间HLA相容程度越高,也就是受者和供者之间HLA-A、B、DR六个位点相合匹配的越多,排斥反应的发生率就越低,移植成功率就越高。反之,就越容易发生排斥反应,对患者术后的生存产生致命的危害。
02、配型为什么困难?
对于干细胞技术,简单来说就是要将供者健康的、正常的干细胞回输到病人体内,来替换病人因疾病丧失功能的病态的、异常的细胞。比如公众广知的新生儿造血干细胞,就是先通过手术或放化疗的处理将体内原有的病态细胞杀死,再将供者的健康细胞输入患者体内。
这个过程中,一旦发生排斥反应,由于受者本身免疫系统通常极为脆弱,极易造成严重后果,引发患者死亡。
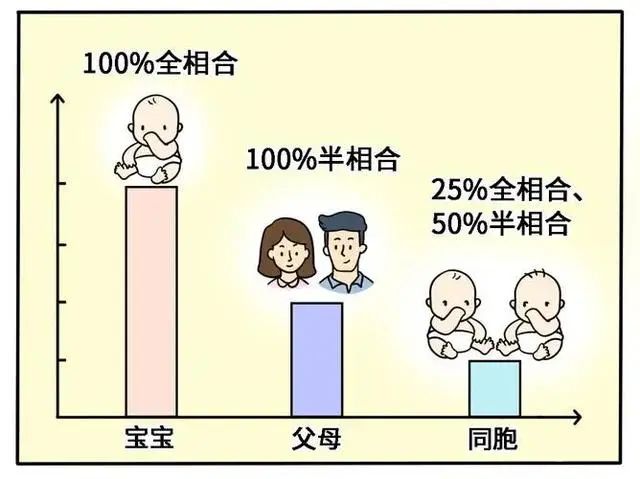
因此,在移植上,通常要求6个位点至少有4个相合。对于亲属来说,患者必然从父亲和母亲中各获得一条染色体,因而与父母的HLA为半相合。而对于兄弟姐妹,根据排列组合有4种情况,与患者有HLA完全一致的可能性为1/4,因此在进行移植时,通常首选在同胞兄妹中找寻供者。
03、胎盘/脐带间充质干细胞为什么无需配型?
胎盘、脐带间充质干细胞,主要指从新生儿胎盘或脐带组织中提取的一种叫做间充质干细胞的细胞。此外还有其它一些免疫相关分子不表达或低表达,这使得间充质干细胞可以逃避机体免疫系统的识别,避开宿主监视,因而回输到体内不会引发很强的排斥反应。因此,在临床上,使用无需进行配型。

另外,胎盘和脐带在发育上非常原始,其来源的间充质干细胞具有很强的免疫调节作用,可以抑制机体亢进的免疫反应,从而防止过度免疫应答可能对宿主组织造成的损伤。
临床上目前已有应用脐带来源的间充质干细胞联合HLA半相合的造血干细胞进行干预,来改善重型再生障碍性贫血,结果发现可以明显降低并发症的发病率,加快造血重建,且降低GVHD(移植物抗宿主病)发生的风险,提高了移植存活率。这对于扩大造血干细胞供者范围,有着重大意义。
04、间充质干细胞成为科学领域研究热点
间充质干细胞是一种多能干细胞,可以向肌腱、血管、神经、脂肪、骨骼等多种组织分化,使其成为再生医学、组织器官损伤退行性疾病治疗领域的研究热点。
从干预的疾病种类来看,间充质干细胞的临床研究涉及上百种疾病。将这些疾病按照器官系统分类,可以发现神经系统、心血管和骨科疾病是三类主要的研究领域,占比都在15%以上,总和超过一半。此外,糖尿病、肝脏、肺脏、胃肠道、皮肤和移植物抗宿主病(GVHD)的比例都在5%左右,是间充质干细胞重要的临床研究方向。
在传统药物针对复杂的疑难疾病时往往束手无策时,间充质干细胞在糖尿病、帕金森综合征、老年痴呆症、肝纤维化、白血病、抗衰老等多种领域均被证明有显著疗效,干细胞研究成果将造福于目前只能靠药物维持的绝症患者,有望引领全新的再生医学革命。
相信,随着未来研究的深入和医疗技术的发展,间充质干细胞的应用前景将更为广阔。






